江苏鑫菲睿生物-五花八门的人工骨,哪些能成为临床不可或缺的骨替代材料
骨组织是一种双相组合材料,一相是以钙磷为主的无机质,一相是以胶原和其他基质构成的有机质。强而硬的无机质包容于弱而易屈的有机质中,使骨具有一定的强度和硬度,并赋予骨特有的生物力学功能,可在人体内担负支持、承重、造血、储钙、代谢等功能。
自体和同种异体骨移植已在临床应用多年。其中自体移植因其移植的骨组织中含有生物活性分子、活细胞,且含有血供,是最理想的骨移植方法,是临床上骨缺损修复的“金标准”。
自体骨移植容易由新骨替代而完成骨缺损的修复,但给患者造成了新的创伤,有一定的并发症,且骨量有限,限制了其在临床的推广应用。
而异体骨移植虽经各种理化处理降低了抗原性,仍有可能引起免疫排斥反应。并且异体移植所带来的潜在疾病的传播,使人们在应用时顾虑重重。继而人们寻求各种人工骨替代材料,来避免自体骨和异体骨的缺点。
人工骨材料通过单独使用或几种材料复合使用来促进骨愈合,其作用原理包括3个方面:
①骨生成作用(osteogenesis),骨生成材料中包含了具有分化成骨潜能的活细胞,具有骨形成作用;
②骨传导作用(osteoconduction),植入材料通过促进宿主骨与移植材料表面的结合,引导骨形成;
③骨诱导作用(osteoinduction),人工骨材料提供一种生物刺激,诱导局部细胞或移植的细胞分化形成成熟的成骨细胞。理想的人工骨在体内应能诱导新骨形成,即诱导间充质干细胞趋化、分化成骨细胞。诱导成骨细胞在局部分泌矿化基质及Ⅰ型胶原蛋白,具有良好的生物学性能,与受体骨有良好的生物相容性。材料可梯度降解,并快速血管化。
寻求理想的骨替代材料、修复骨组织、重建骨的力学和生物学功能,一直是广大学者研究的热点问题。
理想的人工骨替代材料应近似自体移植骨,并能弥补自体骨、异体骨等材料的缺点。其主要性能要求达到:
①植入人体后不产生移植排斥反应和移植物抗宿主反应;
②有骨传导性,能以移植骨为支架,使宿主的血管和细胞进入植骨块形成新骨,随后移植骨降解、吸收并逐渐被新骨替代;
③手术中易于修整,使其轮廓与不同形状的缺损相匹配,必要时材料本身可提供机械支持。如颈椎前路手术时,使用方形的人工骨块可支撑、维持恢复的椎间高度(图4-0-5);最重要的是植入物应能以较低剂量的诱导因子引起最佳的成骨活动,并促使血管及间充质细胞迅速侵入材料,而与吸附在其上的诱导因子接触。
此外,在新骨的生长过程中,材料应逐渐被改建和吸收,并最终从植入部位消失。但迄今为止,各种人工骨替代材料并不能完全达到上述要求。

图4-0-5 用于椎间植骨的羟基磷灰石骨块
目前,临床上应用的骨替代材料按材料属性分为以下几大类:①无机生物材料:包括金属和合金材料、碳素材料、生物活性陶瓷;②有机生物材料:是具有一定生物相容性的合成高聚物材料,主要包括有机硅化合物、聚四氟乙烯、聚丙烯、聚酯类等;③天然生物材料:包括珊瑚、胶原、弹性纤维、透明质酸、甲壳素等。不同的材料其作用原理有所不同。
01
无机材料
1.金属、高分子类
以钛合金为主的金属类材料具有机械强度高、理化性能稳定、生物相容性良好、耐磨损、耐疲劳等特点,作为骨替代材料已广泛应用于临床。钛合金是一种生物惰性材料,缺乏骨诱导性,不能与宿主骨组织化学性结合,仅形成一层致密的纤维包膜。而且弹性模量偏大,机械力学适应性差,易导致应力集中而松动、脱落、失败。因此,金属类材料很少单独使用,常和其他材料复合使用,如椎间融合器(cage)和BMP的联合使用,既保持了cage的支撑作用,又保持了BMP的生物活性,有利于椎体间的融合(图4-0-6)。

图4-0-6 椎间融合器(cage)和BMP的联合使用
高分子聚合物具有与人体组织中天然高分子胶原、纤维粘连素等相似的化学结构,弹性模量亦低于金属、陶瓷,与骨组织的性能更加接近,且生物相容性和机械适应性也较好等优点。但此类材料可引起无菌性炎症,机械强度不足,部分材料的降解产物和残留有机溶剂对机体有一定的毒性,植入后产生纤维囊,降解速度与成骨速度欠协调等缺点。根据植入生物体内的降解情况,分为可降解与非降解两大类,目前临床常用的聚合材料有聚四氟乙烯、聚乳酸、聚乙醇酸、聚甲基丙烯酸甲酯等。
2.生物陶瓷类材料
陶瓷是一种晶体材料,有金属离子和非金属离子两部分,并以离子键相结合。按照其生物活性分为生物惰性陶瓷和生物活性陶瓷。氧化铝等惰性陶瓷缺乏生物活性,不能与宿主骨形成有机的化学界面结合,还常常引起材料下方宿主骨的吸收,已被弃用。在生物活性陶瓷的研究和应用中,以钙磷陶瓷羟基磷灰石和磷酸三钙最为广泛、活跃。它们的主要成分为钙、磷离子,与无机骨相似。其对骨的修复作用主要体现在骨传导性方面,可以为新骨形成提供支架。自体骨的主要化学成分为羟基磷灰石(hydroxylapatite,HA),约占人体骨组织的70%。异种骨、异体骨在脱蛋白后剩下的无机物质即为HA,其HA与人体骨组织结构一致,是临床中常用的一种骨替代材料。羟基磷灰石是一种不吸收的生物活性陶瓷,为晶体结构。摩擦系数及导热性与正常骨相似,具有良好的生物相容性。该物质有骨引导力,能直接与宿主骨形成稳定坚硬的骨性复合体,但缺乏骨诱导性。生物活性陶瓷虽具有良好的生物相容性、化学稳定性及通过离子交换等形式与骨组织发生强有力的化学性结合,但此类材料的最大缺陷是脆性大、抗弯强度低,易于折裂,而且不易吸收。一般仅用于修复需较小负荷的骨缺损,如胫骨平台骨折术后预防关节面塌陷的支撑植骨(图4-0-7),或肿瘤切除后空腔的填充。

图4-0-7 胫骨平台骨折手术前后X线片
(1)术前下陷的胫骨平台;
(2)复位内固定及羟基磷灰石关节面下支撑
02
有机材料
主要包括胶原、α-聚酯及骨生长因子等。胶原与α-聚酯为骨与软骨组织工程中主要的两大生物材料。人工合成的聚合物可以准确地控制其分子量、降解时间以及其他性能,但人工合成材料没有天然材料所包含的许多生物信息(如某些特定的氨基酸序列),不能与细胞发挥理想的相互作用。目前已有将天然材料的某些重要氨基酸序列接在合成聚合物表面的研究,以克服两种材料各自应用的缺陷。多种细胞因子参与并调节骨、软骨的修复,其中骨诱导因子对骨组织的分化起决定性作用。在众多骨生长因子中BMP最受注目,与骨诱导的关系最为密切。BMP通过反馈机制增加向骨系细胞分化的间充质细胞,从而增补新的骨原细胞,再由骨衍生性生长因子刺激这些细胞的有丝分裂,而形成大量新骨。同时,BMP尚能激发肌母细胞转化为骨系细胞,并在骨组织的修复和形成过程中起着重要的调控作用,可用于关节置换术后、创伤、肿瘤或手术造成的骨缺损、骨折的修复和脊柱融合等方面。随着基因工程技术的发展,许多骨生长因子如BMP、bFGF等已能通过人工基因重组产生。但各种生长因子各自的生物学特性,以及多种生长因子联合应用时的成骨效应和释放顺序、骨生长因子的释放方式、应用的安全性、功效及可靠性等,尚需进一步研究。
03
天然生物材料
自1971年人们发现海珊瑚具有与人骨相类似的孔隙结构后,开始应用原始珊瑚碳酸钙作为植骨材料。20多年以来,许多学者的大量研究证实,珊瑚人工骨是一种良好的骨代用品,目前已知它具有良好的生物相容性及骨引导作用,并有生物降解性;其多孔结构有利于宿主骨组织和血液、纤维组织的长入;与骨组织有较强的亲和性;无排斥反应。
但珊瑚骨质地脆,吸收快,在骨缺损处只具有支架和骨引导作用,而无骨诱导能力,单纯珊瑚植入机体后有一定的体积丧失,对于较大的骨质缺损,仅用珊瑚难以达到完全修复。因此,近年来有学者将珊瑚与其他材料进行复合移植,使植骨材料具备骨诱导活性和骨引导活性,并制成各种形状,以满足手术中的需要(图4-0-8)。

图4-0-8 各种形状的珊瑚人工骨1.生物珊瑚与珊瑚-羟基磷灰石复合
植骨材料的降解速度与缺损区骨修复速度的协调一致是至关重要的。降解过快,缺损区即会失去支架作用,不利于骨缺损的完全修复;降解太慢,材料本身会成为新骨形成的障碍,不利于骨缺损的快速修复。在珊瑚的研究过程中,有人发现其在体内的降解速度对于骨缺损的修复速度来说相对稍显过快。
珊瑚-羟基磷灰石(HA)复合材料能与骨组织产生良好的结合,而且不干扰骨形成的生理过程,并对骨缺损的修复有促进作用。珊瑚所特有的微孔结构与骨结构更类似,为宿主骨生长提供有利的生理环境,其在骨缺损的修复中显示了良好的生物学性能。
2.生物珊瑚与自体骨髓复合
早在1869年,Goujon就发现骨髓异位移植后有成骨作用。骨髓由造血干细胞及基质干细胞组成,主要由基质干细胞分化成骨。它含有两种骨母细胞:定向成骨母细胞和诱导成骨母细胞。骨髓细胞通过释放和分泌骨诱导物质,诱导周围非特异性间充质细胞分化成骨,以及骨髓细胞本身分化成骨。
珊瑚骨和自体骨髓复合移植,既为新骨提供支架,又为成骨提供骨诱导物质和成骨细胞,可以加速骨缺损的修复。
3.生物珊瑚与人骨形成蛋白复合
BMP是一种特殊的骨生长因子,在一定条件下,可诱导未分化间叶细胞、骨髓中的骨母细胞和成骨细胞,继而诱导软骨和骨的形成。珊瑚与重组人骨形成蛋白-2(rh-BMP-2)复合,多孔的珊瑚充当rhBMP-2的载体和释放系统,为新骨形成提供支架和空间,是一种较理想的骨移植替代材料。
4.生物珊瑚、胶原和rhBMP-2复合
胶原是一种高分子蛋白质,可制成凝胶状溶液,有一定的黏性,可作为BMP的载体,并能起到缓释BMP的作用。生物珊瑚、胶原和rhBMP-2复合人工骨能引导和诱导新骨形成。
04
非生物性的骨传导材料
可降解聚合物、生物活性玻璃及其他物质等非生物物质作为骨传导材料,其优势在于材料各方面的可控性、无免疫反应及极佳的生物相容性。如聚乳酸和聚乙醇酯可制成各种形状,并与生长因子或其他成分复合制成具有多种功能的载体。可以将其制成泡沫状,使孔径大小最适合骨的长入。尽管骨、软骨能够长入这些聚合物中,但非最佳状态。因此,这些材料的骨传导能力很差。它们的最佳作用是作为药物或生长因子的载体,使其在局部形成高浓度区域。聚合物的降解使因子在局部释放,多数生产泡沫状聚合物的方法都需要加热,这使得大多数生长因子灭活,限制了其在骨科的应用范围。
05
复合人工骨材料
基本原理是将具有骨传导能力的材料与具有骨诱导能力的物质如骨生长因子、骨髓组织等复合制备成复合人工骨,使它们既具有骨传导作用,又具有骨诱导作用。
1.磷酸钙复合人工骨
主要为羟基磷灰石及磷酸三钙与胶原、骨生长因子等组成的复合人工骨。2.聚合物复合人工骨通过技术加工合成各种形态结构,并具有一定生物降解特性的聚合物。但它们无骨诱导活性,需与其他骨诱导因子(如BMP)复合应用,才能诱导新骨的形成。3.红骨髓复合人工骨骨髓由造血系统和基质系统两部分组成。人和动物健康红骨髓的基质细胞中,含有定向性骨原细胞和可诱导性骨原细胞。定向性骨原细胞具有定向分化为骨组织的能力,可诱导性骨原细胞在诱导因子(如BMP)作用下才能分化成骨。红骨髓复合人工骨可为红骨髓提供适宜的诱导分化环境,为骨髓成骨提供有利的场所和条件。其成骨率及成骨量高于单纯移植,能直接促进骨折的愈合和骨缺损的修复。
06
组织工程化人工骨
应用生物学和工程学的原理和方法来发展具有生物活性的人工替代物,以修复、维持或改善病损组织的功能,骨组织工程为骨缺损、骨肿瘤以及难治性骨折的修复提供了一种极有前途的新方法。骨组织工程学是一门以细胞生物学、分子生物学、生物材料学和临床医学等学科为基础的交叉学科,主要包括种子细胞、生长因子、支架材料、三维培养、人工骨修复骨缺损等方面的研究。在此方法中,所使用的细胞载体材料至关重要。一方面,它必须满足各种生物相容性、生物可降解性及力学性能要求;另一方面,它还必须易于制成各种理想的形状,以适于细胞生长、组织再生和脉管形成。由于各单一材料存在明显的缺点,因此近年来组织工程支架材料研制中产生了一个新方法,即应用复合材料的原理,将两种或两种以上具有互补特性的生物材料按一定比例与方式组合,以期构造出能够满足要求的新型复合材料。自20世纪80年代以来,随着材料科学的飞速发展,以生物材料为支架的人工骨为解决这一问题提供了一条新的途径。国际材料学会1996年秋季会议及美国生物材料学会第23届年会指出,骨组织工程应用的战略可分为两种:①将支架材料与细胞因子在体外组装后植入体内,诱导新骨形成;②将成骨细胞在体外种植于材料后植入体内。
07
基因治疗
种子细胞在体外培养过程中,细胞极易老化,从而丧失增殖和分泌基质的能力,同时还存在取材广而细胞培养量少的缺点。局部应用细胞生长因子,也存在生物半衰期短、给药频繁、剂量大而副作用明显、价格昂贵等缺点。随着基因转移(genetransfer)或基因转染(gene transfection)技术的发展,利用转基因技术将组织工程与基因工程完美结合,把生长因子基因作为目的基因引入种子细胞,再将这些细胞与支架材料移植到骨缺损处,使后者成为局部单个生物反应器,获得更强和持续分泌骨生长因子的能力,加速骨形成和修复,将会为骨缺损的治疗提供一个崭新的途径(图4-0-9)。
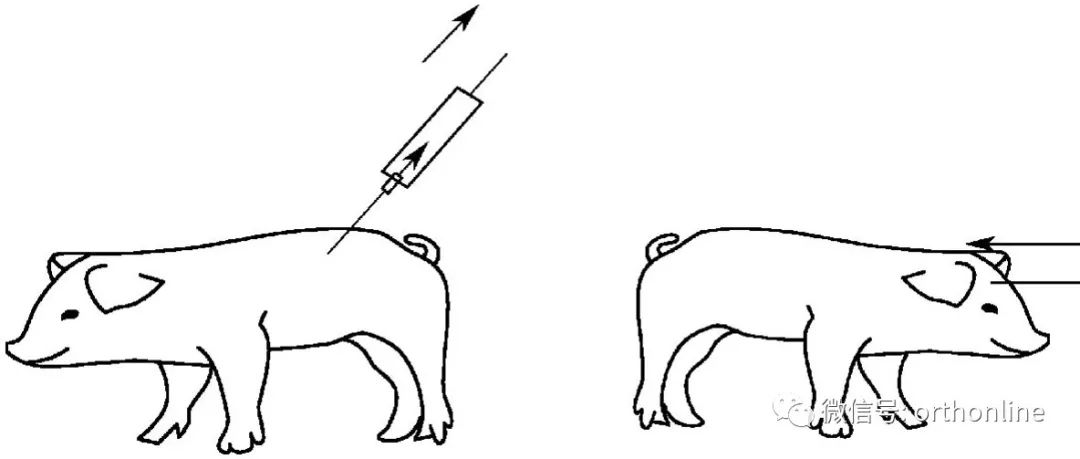
图4-0-9 获取自体骨髓干细胞、体外转染后植入体内修复骨缺损
08
纳米人工骨
纳米科技是在纳米(1nm=10-9m)尺度空间内研究电子、原子、分子运动规律及特性的高新技术。从20世纪90年代初起纳米科技得到了迅速发展,已渗透到各个学科领域,被公认为是21世纪的关键技术。纳米材料是在0.1~100nm尺度空间里具有特定功能的材料,当物质的结构单元(如晶粒或孔隙)小到纳米级时,其性质就会发生重大改变,不仅改善了原来的材料性能,甚致使原材料具有新的性能或效应。纳米多孔陶瓷的孔隙允许新生骨组织的长入,具有诱导成骨作用和良好的机械力学性,比传统材料有更好的生物学性能,能够促进和加快骨缺损的修复。尽管现在临床上有众多的人工合成植骨材料可供选择,但应根据具体的病情、缺损的类型及创面的局部情况选择合适的治疗方法及植骨材料。如对骨折、骨不连或延迟愈合的患者,首先是恢复肢体的力线和局部的稳定,并尽可能保存局部的血运,正常的力学和生物学环境是保证植骨成功的关键。此外,应根据临床治疗中需要解决的问题,如局部骨诱导和(或)骨再生是否存在缺陷、是否需要结构性支撑等来选用相应的植骨材料。
如包容性骨缺损、局部稳定及血运良好者,可选择同种异体骨或磷酸钙类骨替代材料;而对于局部骨形成不良或血运欠佳者则应考虑选择应用自体骨或各种复合人工骨材料,如脱矿物骨基质和自体骨髓的复合移植;大段骨缺损或肿瘤切除后的节段性缺损,为恢复骨骼的支架作用及需要支撑植骨时,则最好选择自体皮质骨或同种异体骨移植。
延伸 · 阅读
- 2024-11-13树立医者典范 礼赞大医精诚 访国宝级中医—周培富
- 2024-11-13解锁华大严选基因的成功密码:特色产品与卓越服务
- 2024-11-12《华大严选生物基因科技有限公司:引领基因科技前沿》
- 2024-11-12见证实力:华大严选基因如何成为行业标杆品牌
- 2024-11-122024年北京十大金牌律师事务所排名:专业与实力的璀璨之星
- 2024-11-12《华大严选基因的传奇:从创立到引领行业的辉煌历程》














